Các doanh nghiệp của Việt Nam đang tiến hành thu hồi tất cả các tên thuốc thành phẩm được sản xuất từ nguyên liệu Valsartan của Trung Quốc.

Ngay sau khi nhận được chỉ đạo của Cục Quản lý Dược, các doanh nghiệp của Việt Nam đang tiến hành thu hồi tất cả các tên thuốc thành phẩm được sản xuất từ nguyên liệu Valsartan của Trung Quốc.
Ngay sau khi nhận được chỉ đạo của Cục Quản lý Dược, Công ty Cổ Phần Dược phẩm Cửu Long đã ngừng ngay việc sử dụng nguyên liệu nói trên trong sản xuất thuốc thành phẩm và ngay lập tức gửi công văn báo cáo đến Cục Quản lý Dược, Bộ Y tế.
Theo đó, số lượng Valsartan nhập về ngày 21/2/2018 là 160 kg, số lượng xuất từ 20/3/2018 đến 31/5/2018 là 49,07 kg. Công ty cổ phần Dược Cửu Long khẳng định tới thời điểm hiện tại, tất cả sản phẩm liên quan này vẫn còn lưu kho và chưa được xuất bán ra thị trường.
Công ty cổ phần Xuất nhập khẩu Y tế Domesco cũng cho biết công ty hiện có 3 loại thuốc thuộc diện thu hồi. Ngay khi nhận được yêu cầu, Domesco đã thông báo tới khách hàng và tiến hành thu hồi toàn bộ sản phẩm mà công ty sản xuất từ nguyên liệu Valsartan của Zhejiang Huahai Pharmaceutical, đồng thời báo cáo về tình hình mua và sử dụng nguyên liệu theo đúng yêu cầu của Cục.
Sau khi sản phẩm bị thu hồi, công ty đã hoàn tất việc nghiên cứu một nguồn nguyên liệu khác để đưa vào sản xuất ngay khi nhận được sự phê duyệt của Cục quản lý Dược, Bộ Y tế.
Giống như Domesco, Pymepharco cũng ngay lặp tức có giải trình về việc thu hồi thuốc. Theo đó, chỉ có Pyvasart 80 có chứa thành phần Valsartan 80mg, Pymepharco đã thu hồi 91.643 viên trên tổng số 817.970 viên được sản xuất. Cái tên còn lại trong 4 công ty đang niêm yết bị buộc thu hồi thuốc là Dược phẩm Trung ương 2 vẫn chưa có phản hồi về vấn đề này.
Ông Nguyễn Văn Khải, Trưởng phòng Nghiệp vụ dược (Sở Y tế Hà Nội) cho biết, Hà Nội có bốn bệnh viện, gồm: Bệnh viện đa khoa Hà Đông, Bệnh viện đa khoa Đống Đa, Bệnh viện Thanh Nhàn và Bệnh viện đa khoa huyện Quốc Oai và ba công ty, gồm: Công ty TNHH Dược phẩm Ba Đình, Công ty TNHH Dược phẩm Gia Minh và Công ty TNHH Dược phẩm Tân An có trúng thầu một số thuốc chứa Valsartan có trong danh mục thuốc được Cục Quản lý Dược cảnh báo.
Hiện tại, ba công ty dược phẩm đã thu hồi được khoảng 136.000 viên thuốc chứa Valsartan trên địa bàn Hà Nội. Bệnh viện đa khoa huyện Quốc Oai chưa nhập thuốc. Bệnh viện Thanh Nhàn đã trả lại cho nhà cung ứng gần 2.000 viên thuốc. Và hai bệnh viện gồm Bệnh viện đa khoa Đống Đa và Bệnh viện đa khoa Hà Đông đã cấp phát hết số thuốc đã nhập.
"Hiện nay, các bệnh viện đã thu hồi 100% nguồn thuốc được phân phối từ ba công ty trên. Vẫn có nhiều thuốc khác cùng hoạt chất đó được lưu hành nên người bệnh yên tâm sẽ có đủ thuốc để sử dụng", ông Khải thông tin.
Lãnh đạo Bệnh viện đa khoa Hà Đông cho hay, trong danh mục thuốc thu hồi mà Cục Quản lý Dược, Bộ Y tế gửi, bệnh viện không nhập khẩu thuốc trực tiếp từ các nhà sản xuất đó.
"Qua kiểm tra thì chúng tôi thấy có một lô thuốc mà chúng tôi nhập khẩu của châu Âu. Nhà sản xuất này lại xác nhận là họ nhập khẩu nguyên liệu từ công ty dược của Trung Quốc. Lô thuốc đó chúng tôi nhập từ tháng 1 và đã cấp phát hết. Hiện nay, khi đã có thông báo của Cục Quản lý Dược như vậy thì chúng tôi sẽ không nhập khẩu thuốc này nữa", vị này cho hay.
Cũng theo lãnh đạo của Bệnh viện đa khoa Hà Đông, hiện điều trị tim mạch, huyết áp có rất nhiều loại thuốc khác nhau, có thành phần và tác dụng tương tự loại thuốc bị thu hồi. Vì vậy, người bệnh có thể yên tâm điều trị.
Có thể bạn quan tâm |
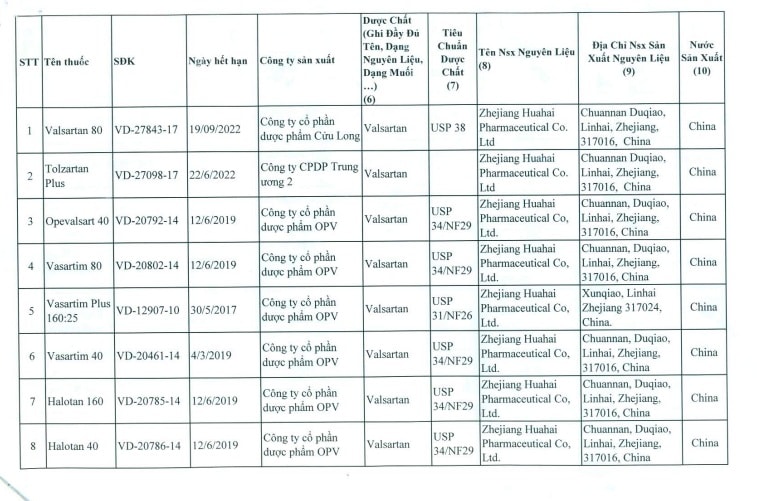
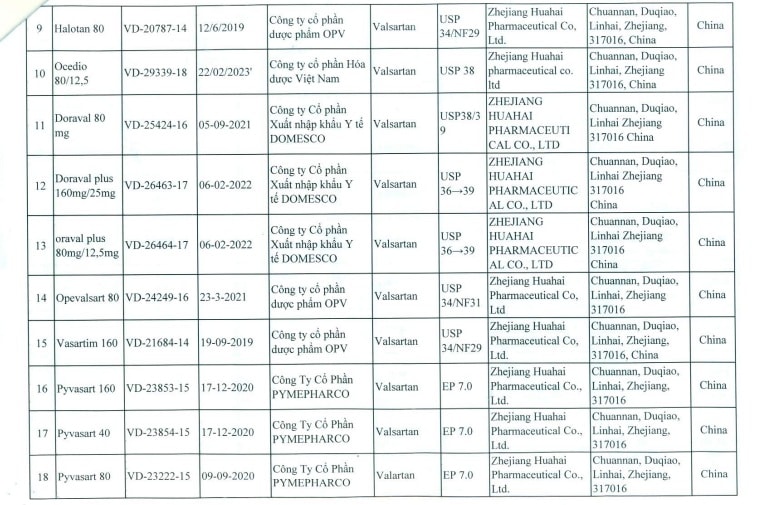
Danh sách 8 doanh nghiệp bị buộc phải thu hồi tất cả các tên thuốc thành phẩm được sản xuất từ nguyên liệu Valsartan của Trung Quốc, gồm:
Công ty CP Dược phẩm Cửu Long (tỉnh Vĩnh Long) thu hồi thuốc Valsartan 80 mg (số đăng ký VD-27843-17).
Công CP Dược phẩm Trung ương 2 (TP Hà Nội) thu hồi thuốc tim mạch Tolzartan Plus 160 mg (số đăng ký VD-27098-17).
Công ty CP Hóa dược Việt Nam (TP Hà Nội) thu hồi thuốc tim mạch Ocedio 80 mg (đăng ký VD-29339-18).
Công ty CP Dược phẩm OPV (tỉnh Đồng Nai) thu hồi 7 loại thuốc trị tim mạch, phù do suy tim và huyết áp, gồm: Opevalsart 40 mg (VD-20792-14), Vasaratim 80mg (VD-20802-14), Vasaratim Plus 160:25 (VD-12907-10), Vasaratim 40 mg (VD-20461-14) và Halotan hoạt chất 40/80/160 mg, Opevalsart 80, Vasaratim 160.
Công ty CP Nhập khẩu Y tế DOMESCO (tỉnh Đồng Tháp) thu hồi 3 thuốc, gồm: Doraval 80 mg (VD-25424-16), Doraval plus 160/25 mg (VD-26463-17), Oraval plus 80/12,5 mg (VD-26464-17).
Công ty CP PYMEPHARCO (tỉnh Phú Yên) thu hồi 4 thuốc Pyvasart hàm lượng 40/80/160 mg và thuốc Pyvasart HCT 80/12.5 mg.
Công ty TNHH Liên doanh STADA Việt Nam (TP HCM) thu hồi 4 thuốc Valsartan STADA hàm lượng 40/80/160 mg và chi nhánh của công ty ở Bình Dương thu hồi 2 thuốc Valsartan STADA 40 mg, Valsartan STADA 80 mg.
Danh sách đình chỉ lưu hành tất cả các thuốc thành phẩm được sản xuất từ nguyên liệu Valsartan do Công ty Zhejiang Huahai Pharmaceutical của Trung Quốc sản xuất: